Hva er en mRNA-vaksine
mRNA-vaksinen overfører RNA til cellene i kroppen for å uttrykke og produsere proteinantigener etter relevante modifikasjoner in vitro, og dermed føre til at kroppen produserer en immunrespons mot antigenet, og utvider dermed kroppens immunkapasitet.[1,3].
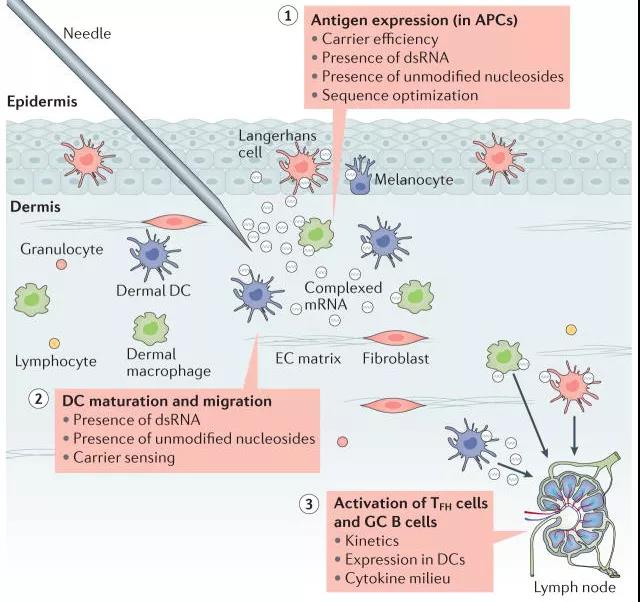
Figur 1: Skjematisk diagram av effekten av direkte injeksjon av mRNA-vaksine [2]
Klassifisering av mRNA-vaksiner
mRNA-vaksiner er delt inn i to typer:ikke-replikerendemRNA ogselvforsterkendemRNA: selvamplifiserende mRNA koder ikke bare for målantigenet, men koder også for replikasjonen som muliggjør intracellulær RNA-amplifisering og proteinekspresjonsmekanisme.Ikke-replikerende mRNA-vaksiner koder kun for målantigener og inneholder 5'- og 3'-utranslaterte regioner (UTR).De gir omfattende stimulering av tilpasningsevne og medfødt immunitet, nemlig in situ antigenekspresjon og faresignaloverføring, og har følgende applikasjoner Funksjoner[2,3]
●Kan gi omfattende stimulering av tilpasningsevne og medfødt immunitet, nemlig in situ antigenekspresjon og faresignaloverføring
●Kan indusere en "balansert" immunrespons, inkludert humorale og cellulære effektorer og immunminne
●Kan kombinere forskjellige antigener uten å øke kompleksiteten i vaksineformuleringen
●Kontinuerlig forbedring av immunpotensialet kan oppnås gjennom gjentatt vaksinasjon, og det er ingen eller liten immunrespons mot bæreren
●Varmestabile mRNA-vaksiner kan forenkle transport og lagring av vaksiner
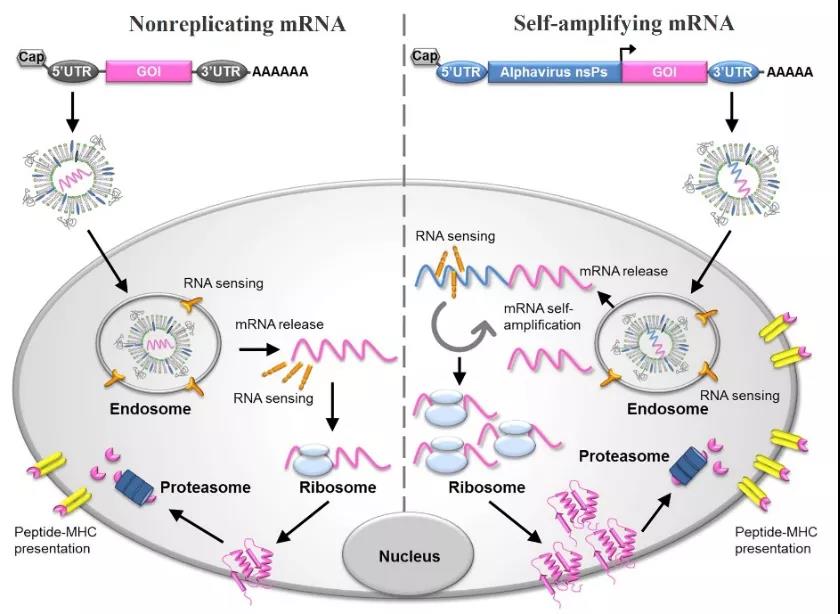
Figur 2: Skjematisk diagram av mRNA-vaksine og dens antigenekspresjonsmekanisme [4]
Funksjoner av mRNA-vaksiner
Sammenlignet med tradisjonelle vaksiner har mRNA-vaksiner enkle produksjonsprosesser, raske utviklingshastigheter, ikke behov for cellekultur og lave kostnader.Sammenlignet med DNA-vaksiner trenger ikke mRNA-vaksiner å komme inn i kjernen og det er ingen risiko for integrering i vertsgenomet.Halveringstiden kan justeres ved modifikasjon.
Tabell 1: Fordeler og ulemper med mRNA-vaksiner
|
| Fordel | Mangel |
| mRNA-vaksine | Rask forskning og utvikling, vaksineproduksjon tar bare 40 dager | Utløse en unødvendig immunrespons
|
| mRNA-ustabilitet under fysiologiske forhold, lett å bryte ned | Vil ikke integreres i genomet for å unngå mulige terapeutiske mutasjoner
| |
| Ikke behov for noe kjernefysisk lokaliseringssignal, transkripsjon | Effektiviteten til sikkerhetsatomkraftverket gjenstår å verifisere
|
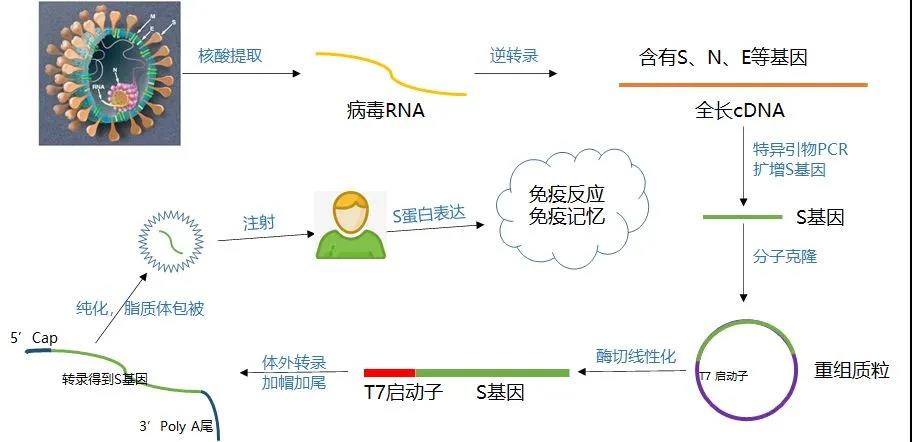
Figur 3: Flytskjema over produksjon og klargjøring av mRNA-vaksine [4]
Foregene viral RNA isolasjonssett
RT-qPCR Enkel (ett trinn)
Forbedrede strategier for fremstilling av mRNA-vaksiner
På grunn av den dårlige stabiliteten til mRNA i seg selv, enkel nedbrytning av nukleaser i vev, lav celleinngangseffektivitet og lav translasjonseffektivitet, begrenser disse defektene bruken av mRNA-vaksiner.Oversettelseseffektivitet spiller også en svært kritisk rolle.Leveringsbærere kan deles inn i virale vektorer og ikke-virale vektorer (inkludert liposomer, ikke-liposomer, virus, nanopartikler, etc.).Det er derfor behov for relevante forbedringstiltak.Følgende er en farmakologisk forbedringsstrategi for mRNA-preparat[2]
1 Syntetiser cap-analoger eller bruk avgrensningsenzymer for å stabilisere mRNA og øke proteintranslasjonen ved å binde seg til eukaryot translasjonsinitieringsfaktor 4E (EIF4E)
2 Juster elementene i den 5′-utranslaterte regionen (UTR) og 3′-UTR for å stabilisere mRNA og øke proteintranslasjonen
3 Tilsetning av Poly(A)-hale kan stabilisere mRNA og øke proteinoversettelse
4 Modifiserte nukleosider for å redusere medfødt immunaktivering og øke translasjonen
5 Behandling med RNase III og rask proteinvæskekromatografi (FPLC) rensing kan redusere immunaktivering og øke translasjonen
6 Optimaliser sekvenser eller kodoner for å øke translasjonen
7 Samlevering av translasjonsinitieringsfaktorer og andre metoder for å endre translasjon og immunogenisitet
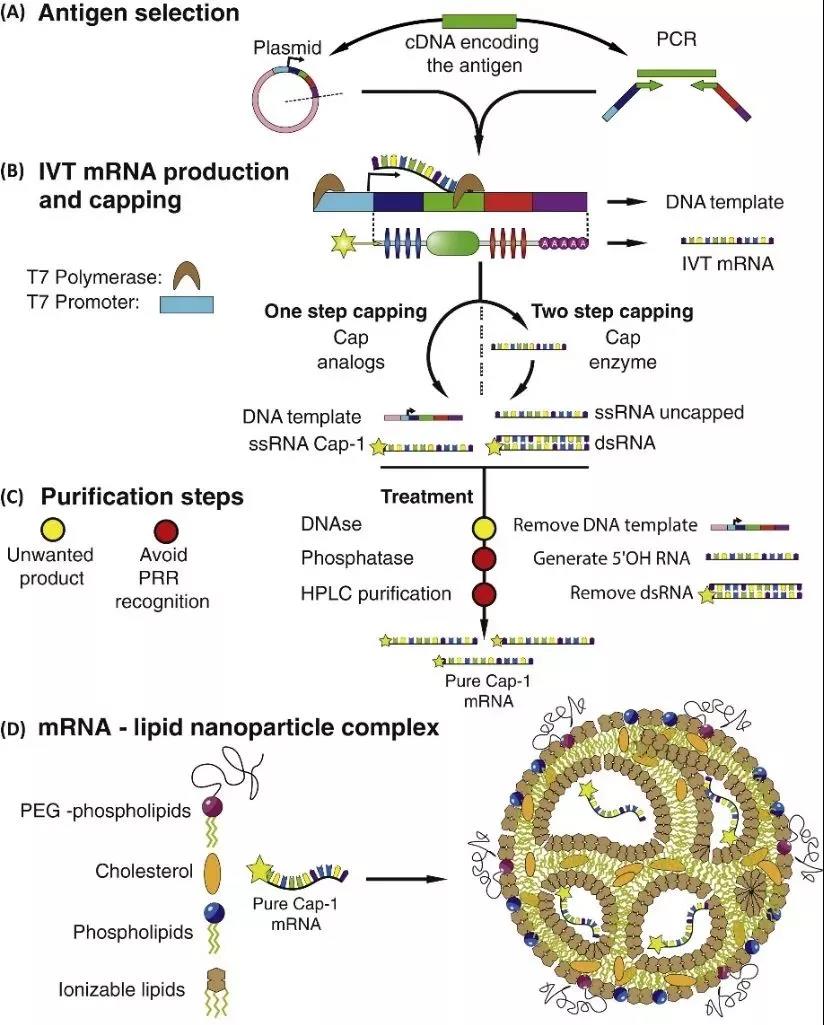
Figur 4: In vitro transkripsjon (IVT) mRNA produksjon og monteringsprosess [5]
Storskala fremstilling av plasmid DNA
Plasmid-DNA-rensing fjerner hovedsakelig forurensninger som RNA, åpensirkel-DNA-endotoksin, vertsprotein og vertsnukleinsyre, og transformerer vanligvis rekombinant plasmid til E. coli.E. coli gjennomgår gjæring med høy tetthet, deretter fast-væske-separasjon og innsamling av E. coli.E. coli utsettes deretter for alkalisk lyse, sentrifugal faststoff-væske-separasjon og mikrofiltreringsklaring etter lysering, ultrafiltrering og konsentrering etter klaring, og deretter kromatografisk rensing.

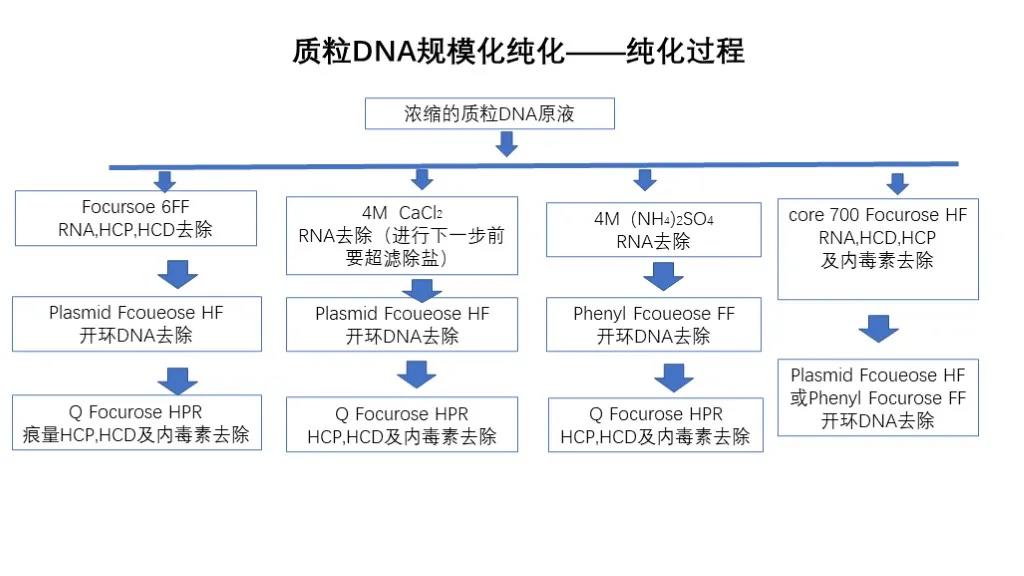
Rensing av plasmid DNA:
Foregene General Plasmid Mini Kit
【1】苗鹤凡, 郭勇, 江新香.mRNA疫苗研究进展及挑战[J].免疫学杂志, 2016(05):446-449.
【2】Pardi N, Hogan MJ, Porter FW, et al.mRNA-vaksiner — en ny æra innen vaksinologi[J].Nature Reviews Drug Discovery, 2018.
【3】Kramps T., Elbers K. (2017) Introduksjon til RNA-vaksiner.I: Kramps T., Elbers K. (red) RNA Vaccines.Methods in Molecular Biology, vol 1499. Humana Press, New York, NY.
【4】Maruggi G, Zhang C, Li J, et al.mRNA som en transformativ teknologi for vaksineutvikling for å kontrollere infeksjonssykdommer[J].Molekylær terapi, 2019.
【5】Sergio Linares-Fernández, Céline Lacroix,, Skreddersy mRNA-vaksine for å balansere medfødt/adaptiv immunrespons, Trender i molekylær medisin, bind 26, utgave 3,2020, side 311-323.
Innleggstid: Aug-05-2021








