1. Grunnleggende kunnskap (hvis du vil se den eksperimentelle delen, vennligst overfør direkte til den andre delen)
Som en derivatreaksjon av konvensjonell PCR, overvåker sanntids-PCR hovedsakelig endringen av mengden amplifikasjonsprodukt i hver syklus av PCR-amplifikasjonsreaksjonen i sanntid gjennom endringen av fluorescenssignalet, og kvantitativt analyserer startmalen gjennom forholdet mellom ct-verdien og standardkurven.
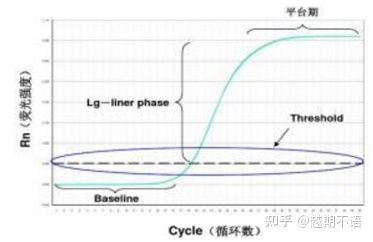
De spesifikke dataene for RT-PCR ergrunnlinje, fluorescensterskelogCt-verdi.
| grunnlinje: | Fluorescensverdien for 3.-15. syklus er grunnlinjen (grunnlinje), som er forårsaket av en og annen feil i målingen. |
| Terskel (terskel): | Refererer til fluorescensdeteksjonsgrensen satt til en passende posisjon i den eksponentielle vekstregionen av amplifikasjonskurven, vanligvis 10 ganger standardavviket til grunnlinjen. |
| CT-verdi: | Det er antall PCR-sykluser når fluorescensverdien i hvert reaksjonsrør når terskelen. Ct-verdien er omvendt proporsjonal med mengden initialmal. |
Vanlige merkingsmetoder for RT-PCR:
| metode | fordel | mangel | anvendelsesområde |
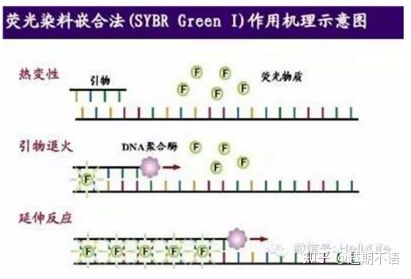
| SYBR GrønnⅠ | Bred anvendelighet, følsom, billig og praktisk | Primerkravene er høye, utsatt for uspesifikke bånd | Den er egnet for kvantitativ analyse av ulike målgener, forskning på genuttrykk og forskning på transgene rekombinante dyr og planter. |
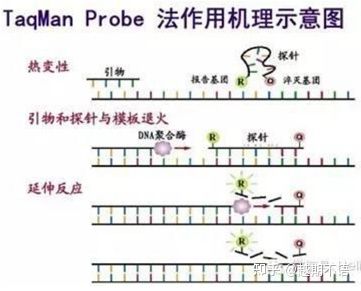
| TaqMan | God spesifisitet og høy repeterbarhet | Prisen er høy og passer kun for spesifikke mål. | Patogendeteksjon, medikamentresistens-genforskning, vurdering av legemiddeleffektivitet, diagnostisering av genetiske sykdommer. |
| molekylært fyrtårn | Høy spesifisitet, fluorescens, lav bakgrunn | Prisen er høy, den er kun egnet for et bestemt formål, designet er vanskelig, og prisen er høy. | Spesifikk genanalyse, SNP-analyse |
2. Eksperimentelle trinn
2.1 Om forsøksgrupperingen- det må være flere brønner i gruppen, og det må være biologiske repetisjoner.
| ① | Tom kontroll | Brukes til å oppdage cellevekststatus i eksperimenter |
| ② | Negativ kontroll siRNA (ikke-spesifikk siRNA-sekvens) | Demonstrere spesifisiteten til RNAi-handling.siRNA kan indusere ikke-spesifikk stressrespons ved en konsentrasjon på 200nM. |
| ③ | Transfeksjonsreagenskontroll | Utelukk toksisiteten til transfeksjonsreagenset til cellene eller effekten på ekspresjonen av målgenet |
| ④ | siRNA mot målgenet | Slå ned uttrykket av målgenet |
| ⑤ (valgfritt) | positiv siRNA | Brukes til å feilsøke eksperimentelle system- og driftsproblemer |
| ⑥ (valgfritt) | Fluorescerende kontroll siRNA | Effektiviteten av celletransfeksjon kan observeres med et mikroskop |
2.2 Prinsipper for primerdesign
| Amplifisert fragmentstørrelse | Helst ved 100-150bp |
| Primer Lengde | 18-25 bp |
| GC innhold | 30%-70%, fortrinnsvis 45%-55% |
| Tm verdi | 58–60 ℃ |
| Sekvens | Unngå T/C kontinuerlig;A/G kontinuerlig |
| 3 sluttsekvens | Unngå GC-rik eller AT-rik;terminalbasen er fortrinnsvis G eller C;det er best å unngå T |
| Komplementaritet | Unngå komplementære sekvenser på mer enn 3 baser i primeren eller mellom to primere |
| Spesifisitet | Bruk blast-søk for å bekrefte primerspesifisitet |
①SiRNA er artsspesifikk, og sekvensene til forskjellige arter vil være forskjellige.
②SiRNA er pakket i frysetørket pulver, som kan lagres stabilt i 2-4 uker ved romtemperatur.
2.3 Verktøy eller reagenser som må forberedes på forhånd
| Primer (intern referanse) | Inkludert forover og bakover to |
| Primere (målgen) | Inkludert forover og bakover to |
| Mål Si RNA (3 strimler) | Vanligvis vil selskapet syntetisere 3 strimler, og deretter velge en av de tre ved RT-PCR |
| Transfeksjonssett | Lipo2000 osv. |
| RNA Rapid Extraction Kit | For RNA-ekstraksjon etter transfeksjon |
| Rask omvendt transkripsjonssett | for cDNA-syntese |
| PCR amplifikasjonssett | 2×Super SYBR Grønn qPCR Master Mix |
2.4 Angående problemene som må tas hensyn til i de spesifikke eksperimentelle trinnene:
①siRNA transfeksjonsprosess
1. For plating kan du velge 24-brønns plate, 12-brønns plate eller 6-brønns plate (den gjennomsnittlige RNA-konsentrasjonen foreslått i hver brønn i en 24-brønns plate er ca. 100-300 ng/uL), og den optimale transfeksjonstettheten av celler er opptil 60 % -80 % eller så.
2. Transfeksjonstrinnene og spesifikke krav er strengt i samsvar med instruksjonene.
3. Etter transfeksjon kan prøver tas innen 24-72 timer for mRNA-deteksjon (RT-PCR) eller proteindeteksjon innen 48-96 timer (WB)
② RNA-ekstraksjonsprosess
1. Forhindre kontaminering med eksogene enzymer.Det inkluderer hovedsakelig bruk av masker og hansker strengt tatt;ved hjelp av steriliserte pipettespisser og EP-rør;vannet som brukes i eksperimentet må være RNase-fritt.
2. Det anbefales å gjøre to ganger som foreslått i hurtigekstraksjonssettet, som virkelig vil forbedre renheten og utbyttet.
3. Avfallsvæsken må ikke berøre RNA-kolonnen.
③ RNA kvantifisering
Etter at RNA er ekstrahert, kan det kvantifiseres direkte med Nanodrop, og minimumsavlesningen kan være så lav som 10ng/ul.
④Revers transkripsjonsprosess
1. På grunn av den høye sensitiviteten til RT-qPCR, bør det lages minst 3 parallelle brønner for hver prøve for å forhindre at den påfølgende Ct blir for forskjellig eller SD-en for stor for statistisk analyse.
2. Ikke frys og tin Mastermix gjentatte ganger.
3. Hvert rør/hull må byttes ut med en ny spiss!Ikke bruk den samme pipettespissen kontinuerlig for å legge til prøver!
4. Filmen festet til 96-brønnsplaten etter tilsetning av prøven må jevnes med en plate.Det er best å sentrifugere før du setter det på maskinen, slik at væsken på rørveggen kan strømme ned og fjerne luftbobler.
⑤ Felles kurveanalyse
| Ingen periode med logaritmisk vekst | Muligens høy konsentrasjon av mal |
| Ingen CT-verdi | Feil trinn for å oppdage fluorescerende signaler; nedbrytning av primere eller prober – dens integritet kan påvises ved PAGE-elektroforese; utilstrekkelig mengde mal; nedbrytning av maler – unngå innføring av urenheter og gjentatt frysing og tining i prøvepreparering; |
| Ct>38 | Lav forsterkningseffektivitet;PCR-produktet er for langt;ulike reaksjonskomponenter brytes ned |
| Lineær forsterkningskurve | Prober kan bli delvis degradert ved gjentatte fryse-tine-sykluser eller langvarig eksponering for lys |
| Forskjellen i dupliserte hull er spesielt stor | Reaksjonsløsningen er ikke fullstendig smeltet eller reaksjonsløsningen er ikke blandet;termalbadet til PCR-instrumentet er forurenset av fluorescerende stoffer |
2.5 Om dataanalyse
Dataanalysen av qPCR kan deles inn i relativ kvantifisering og absolutt kvantifisering.For eksempel, celler i behandlingsgruppen sammenlignet med celler i kontrollgruppen,
Hvor mange ganger X-genets mRNA endres, er dette relativ kvantifisering;i et visst antall celler, mRNA til X-genet
Hvor mange eksemplarer det er, dette er absolutt kvantifisering.Vanligvis er det vi bruker mest i laboratoriet den relative kvantitative metoden.Som oftest,2-ΔΔct-metodenbrukes mest i eksperimenter , så bare denne metoden vil bli introdusert i detalj her.
2-ΔΔct metode: Resultatet oppnådd er forskjellen i ekspresjonen av målgenet i forsøksgruppen i forhold til målgenet i kontrollgruppen.Det kreves at amplifikasjonseffektiviteten til både målgenet og det interne referansegenet er nær 100 %, og det relative avviket bør ikke overstige 5 %.
Beregningsmetoden er som følger:
Δct kontrollgruppe = ct verdi av målgen i kontrollgruppe – ct verdi av internt referansegen i kontrollgruppe
Δct eksperimentell gruppe = ct-verdi for målgenet i eksperimentell gruppe – ct-verdi for det interne referansegenet i den eksperimentelle gruppen
ΔΔct=Δct eksperimentell gruppe-Δct kontrollgruppe
Til slutt, beregne multiplum av forskjellen i uttrykksnivå:
Change Fold=2-ΔΔct (tilsvarende excel-funksjonen er POWER)
Relaterte produkter:
Innleggstid: 20. mai 2023